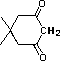|
Nome corrente |
Formula |
Costante di aciditŕ |
pKa |
acido trifluorometansolfonico |
CF3SO3H |
ca. 1013 |
ca. -13 |
acido benzensolfonico |
C6H5SO3H |
ca. 103 |
ca. -2.5 |
acido metansolfonico |
CH3SO3H |
ca. 3 * 102 |
ca. -2.0 |
acido trifluoroacetico |
CF3CO2H |
1.0 |
0.0 |
acido picrico |
(O2N)3C6H2OH |
0.5 |
0.3 |
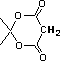
acido squarico |
|
K1 = 0.33 |
1.5 |
|
acido tricloroacetico |
CCl3CO2H |
0.23 |
0.77 |
acido ossalico |
(CO2H)2 |
K1 = 6.5 * 10-2
|
1.2 |
|
acido dicloroacetico |
CHCl2CO2H |
5.5 * 10-2 |
1.25 |
|
acido fluoroacetico |
FCH2CO2H |
2.5 * 10-3 |
2.6 |
|
acido cloroacetico |
ClCH2CO2H |
1.36 * 10-3 |
2.87 |
|
acido citrico |
C(OH)(CH2CO2H)2CO2H |
K1 = 7.4 * 10-4
|
3.13 |
|
acido formico |
HCO2H |
1.77 * 10-4 |
3.75 |
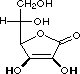
acido ascorbico |
|
K1 = 6.7 * 10-5
|
4.17 |
|
acido benzoico |
C6H5CO2H |
6.3 * 10-5 |
4.20 |
|
acido acetico |
CH3CO2H |
1.77 * 10-5 |
4.75 |
|
tiofenolo |
C6H5SH |
2.5 * 10-7 |
6.6 |
|
tropolone |
|
2.0 * 10-7 |
6.7 |
|
p-nitrofenolo |
O2NC6H4OH |
5.7 * 10-8 |
7.2 |
|
acido peracetico |
CH3COO2H |
5.7 * 10-9 |
8.2 |
|
succinimmide |
(CH2CO)2NH |
2.5 * 10-10 |
9.6 |
|
fenolo |
C6H5OH |
10-10 |
10.0 |
|
idrato di cloralio |
CCl3CH(OH)2 |
10-10 |
10.0 |
|
benzenesolfonammide |
C6H5SO2NH2 |
8 * 10-11 |
10.1 |
|
2-idrossi-2-cicloesenone |
|
5.0 * 10-11 |
10.3 |
|
etantiolo |
C2H5SH |
2.5 * 10-11 |
10.6 |
|
acetossima |
(CH3)2C=NOH |
6 * 10-13 |
12.2 |
|
2,2,2-trifluoroetanolo |
CF3CH2OH |
4 * 10-13 |
12.4 |
|
imidazolo |
C3H3N2H |
3.3 * 10-15 |
14.5 |
|
pirrolo |
C4H4NH |
10-15 |
15 |
|
etanolo |
C2H5OH |
10-16 |
16 |
|
1°-ammide |
RCONH2 |
10-17 |
17 |
|
p-nitroanilina |
O2NC6H4NH2 |
3.3 * 10-19 |
18.5 |
t-butanolo |
(CH3)3COH |
10-19 |
19 |
anilina |
C6H5NH2 |
10-27 |
27 |
1,1,1,3,3,3,-esametildisilazano |
[(CH3)3Si]2NH |
10-30 |
30 |
pirrolidina |
C4H8NH |
10-32 |
32 |
diisopropilammina |
[(CH3)2CH]2NH |
1.9 * 10-36 |
35.7 |
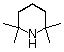
tetrametilpiperidina |
|
10-37 |
37 |
Michigan State University |